La hidrólisis de un éster es el proceso químico mediante el cual un éster reacciona con agua, descomponiéndose en un ácido carboxílico y un alcohol. Este proceso puede ocurrir bajo condiciones ácidas o básicas:
Objetivo de aprendizaje
Analizar el proceso de la hidrólisis de ésteres, y entender su importancia en la química y en aplicaciones industriales.
1. Hidrólisis de ésteres
Hidrólisis Ácida (Hidrólisis Acida): En presencia de un ácido, el éster se convierte primero en un ion éster protonado, lo cual facilita la ruptura del enlace entre el carbono del carbónilo y el oxígeno del grupo alcoxi. La reacción es típicamente reversible, lo que significa que las concentraciones de reactantes y productos alcanzan un equilibrio.
Ecuación general de la reacción:
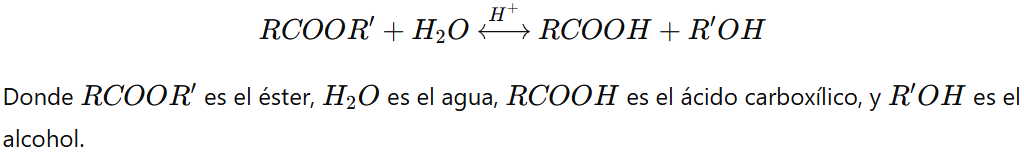
Hidrólisis Básica (Saponificación): En un medio básico, la hidrólisis es típicamente irreversible. El hidróxido de sodio o de potasio reacciona con el éster para formar un alcohol y la sal del ácido carboxílico (jabón en el caso de ácidos grasos).
Ecuación general de la reacción:
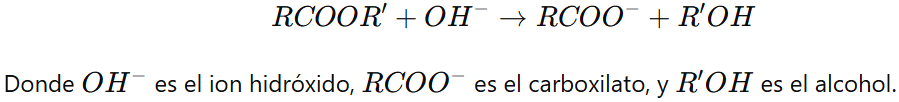
2. Usos e importancia de la hidrólisis de ésteres
- Producción de Jabones y Detergentes: La saponificación de grasas y aceites naturales con bases fuertes produce jabones, un proceso de hidrólisis básica de ésteres.
- Síntesis Química: La hidrólisis de ésteres es un método importante para obtener ácidos carboxílicos y alcoholes, que son intermedios valiosos en la síntesis de diversos compuestos químicos.
- Industria Alimentaria: Los ésteres que contribuyen a los sabores y aromas de los alimentos pueden hidrolizarse, afectando las propiedades de sabor durante el procesamiento y almacenamiento de alimentos.
- Procesos Biológicos: La hidrólisis enzimática de ésteres en el cuerpo juega un papel crucial en la digestión y el metabolismo de lípidos.
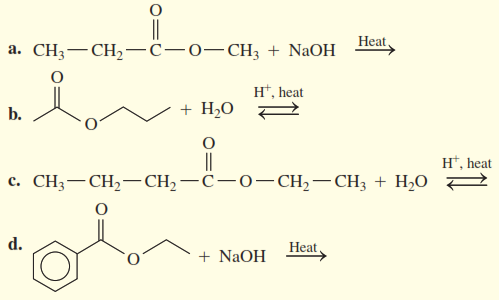
Ejercicios de práctica
1. Dibuja las fórmulas estructurales condensadas para los productos de la hidrólisis catalizada por ácido o base de cada uno de los siguientes: