Los nitrilos son compuestos orgánicos que contienen el grupo funcional -C≡N (un triple enlace entre carbono y nitrógeno). Son compuestos esenciales en la química orgánica debido a su reactividad y versatilidad en diversas reacciones de síntesis.
Los nitrilos se pueden obtener de varias maneras y se encuentran en la naturaleza como intermediarios en la biosíntesis de otros compuestos importantes, como los aminoácidos y las vitaminas. Además, tienen una amplia gama de aplicaciones industriales, que incluyen la fabricación de polímeros, plásticos, y como intermediarios en la síntesis de productos farmacéuticos.
Objetivo de aprendizaje
Identificar las propiedades y usos de los nitrilos, y comprender su comportamiento químico en reacciones orgánicas.
1. Propiedades de los nitrilos
Los nitrilos son compuestos orgánicos que contienen el grupo cianuro (-C≡N) unido a un carbono en una estructura de triple enlace. Este grupo funcional tiene un átomo de nitrógeno unido a un carbono, que puede estar en una cadena alifática o aromática. La fórmula general de un nitrilo es R-C≡N, donde R puede ser un grupo alquilo, arilo o cualquier otro grupo sustituyente.
Propiedades:
- Polaridad: Los nitrilos son compuestos polares debido a la diferencia de electronegatividad entre el carbono y el nitrógeno en el grupo cianuro. Esto da lugar a un dipolo, lo que hace que los nitrilos sean solubles en disolventes polares como el agua y los alcoholes, aunque la solubilidad disminuye a medida que el tamaño de la cadena hidrocarbonada R aumenta.
- Punto de ebullición: Los nitrilos tienen puntos de ebullición relativamente altos en comparación con los hidrocarburos de tamaño similar debido a la polaridad del grupo cianuro, que puede generar interacciones dipolo-dipolo entre las moléculas.
- Reactividad: El grupo -C≡N es bastante reactivo y participa en una variedad de reacciones orgánicas. Los nitrilos pueden sufrir una hidrolización para formar ácidos carboxílicos o amidas, dependiendo de las condiciones, o pueden reaccionar con reactivos nucleofílicos en reacciones como la adición nucleofílica.
- Toxicidad: Los nitrilos pueden ser tóxicos debido a la presencia del grupo cianuro. Este grupo tiene la capacidad de liberar cianuro libre bajo ciertas condiciones, lo que puede ser peligroso para los seres vivos. Por ello, su manejo debe ser cuidadoso.
- Estabilidad: Los nitrilos son relativamente estables bajo condiciones normales, pero se pueden hidrolizar a ácido carboxílico en presencia de agua y calor, especialmente en condiciones ácidas o básicas.
2. Usos de los nitrilos
- Intermediarios en la síntesis de productos químicos: Los nitrilos son intermediarios importantes en la síntesis de una amplia gama de productos químicos, incluidos los ácidos carboxílicos, amidas, aminoácidos y vitaminas. Uno de los ejemplos más comunes es la conversión de nitrilos a ácidos carboxílicos mediante hidrolización.
- Fabricación de Polímeros: Los nitrilos, en especial el acrilonitrilo (C₃H₃N), se utilizan en la fabricación de plásticos como el polímero acrílico. El acrilonitrilo se usa para producir polímeros acrílicos y polímeros de nitrilo butadieno (NBR), que son materiales clave en la producción de cauchos sintéticos, sellos y otros productos industriales.
- Solventes y productos industriales: Algunos nitrilos, como el acetonitrilo (CH₃CN), se emplean como solventes orgánicos en la industria química y farmacéutica, debido a su capacidad para disolver una amplia gama de compuestos polares y no polares. Además, se utilizan en la producción de fármacos y agroquímicos.
- Fabricación de productos farmacéuticos: Los nitrilos y sus derivados juegan un papel clave en la fabricación de productos farmacéuticos, ya que muchos compuestos bioactivos contienen un grupo nitrilo como parte de su estructura química. Estos compuestos pueden ser utilizados en la síntesis de fármacos para el tratamiento de diversas enfermedades, como anticancerígenos o agentes antimicrobianos.
- Síntesis de Aminoácidos y Proteínas: Los nitrilos también pueden actuar como intermediarios en la biosíntesis de aminoácidos esenciales, que son los bloques de construcción de las proteínas. Por ejemplo, algunos nitrilos pueden hidrolizarse a ácidos carboxílicos, que luego se convierten en aminoácidos.
3. Nomenclatura de nitrilos
La IUPAC nombra los nitrilos añadiendo el sufijo -nitrilo al nombre del alcano con igual número de carbonos.
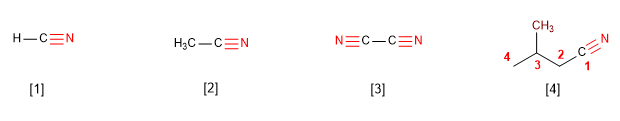
[1] Metanonitrilo
[2] Etanonitrilo
[3] Etanodinitrilo
[4] 3-Metilbutanonitrilo
Cuando actúan como sustituyentes se emplea la partícula ciano-….., precediendo el nombre de la cadena principal.

[5] Ácido 3-Bromo-5-cianohexanoico
[6] Ácido 3-cianociclohexanocarboxílico
Los nitrilos unidos a ciclos se nombran terminando el nombre del anillo en -carbonitrilo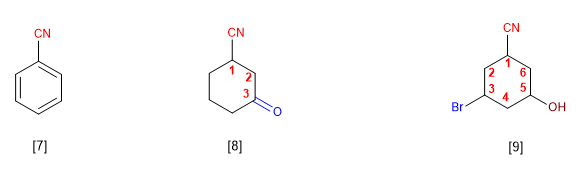
[7] Bencenocarbonitrilo (Benzonitrilo)
Ejercicios de práctica
1. Escriba la nomenclatura para las siguientes estructuras:
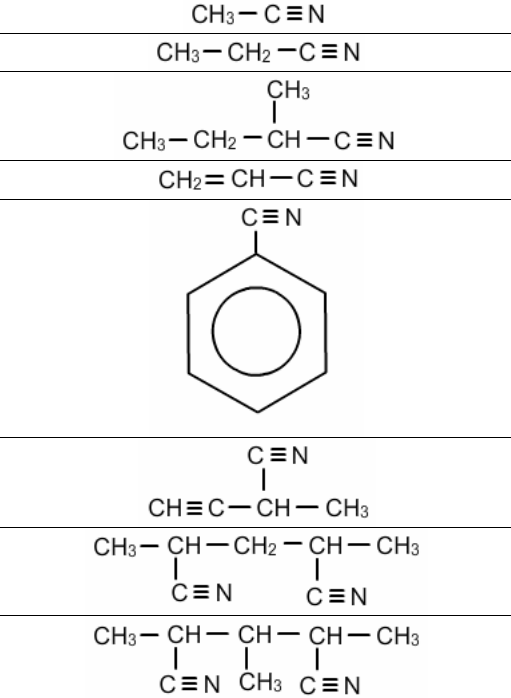
2. Represente las estructuras condensadas para los siguientes compuestos:
a) Propanodinitrilo
b) 2-pentenonitrilo
c) Cianuro de isobutilo
d) Cianuro de 2,3-hexadienilo
e) Benzonitrilo
f) Acetonitrilo
g) 2-etil-3-metilciclopentanocarbonitrilo
h) 1-propeno-1,2,3-tricarbonitrilo
i) 3-cianoanilina
j) 2-etil-3-isopropilbutanonitrilo
