Muchos tipos de alcanos son componentes de los combustibles que impulsan nuestros automóviles y del aceite que calienta nuestros hogares. Puede que hayas utilizado una mezcla de hidrocarburos, como el aceite mineral, como laxante o vaselina para suavizar tu piel. Las diferencias en los usos de muchos de los alcanos se deben a sus propiedades físicas, incluyendo la solubilidad y la densidad.
Objetivo de aprendizaje
- Identificar las propiedades de los alcanos y escribir una ecuación química balanceada para la combustión.
1. Algunos usos de los alcanos
Los primeros cuatro alcanos—metano, etano, propano y butano—son gases a temperatura ambiente y se utilizan ampliamente como combustibles para calefacción.
Los alcanos que tienen de cinco a ocho átomos de carbono (pentano, hexano, heptano y octano) son líquidos a temperatura ambiente. Son altamente volátiles, lo que los hace útiles en combustibles como la gasolina.
Los alcanos líquidos con 9 a 17 átomos de carbono tienen puntos de ebullición más altos y se encuentran en el queroseno, diésel y combustibles para aviones. El aceite de motor es una mezcla de hidrocarburos líquidos de alto peso molecular y se utiliza para lubricar los componentes internos de los motores. El aceite mineral es una mezcla de hidrocarburos líquidos y se utiliza como laxante y lubricante.
Los alcanos con 18 o más átomos de carbono son sólidos cerosos a temperatura ambiente. Conocidos como parafinas, se usan en recubrimientos cerosos añadidos a frutas y verduras para retener la humedad, inhibir el moho y mejorar la apariencia. La vaselina es una mezcla semisólida de hidrocarburos con más de 25 átomos de carbono utilizada en ungüentos, cosméticos y como lubricante.
2. Solubilidad y densidad
Los alcanos son no polares, lo que los hace insolubles en agua. Sin embargo, son solubles en solventes no polares como otros alcanos. Los alcanos tienen densidades que van de 0,62 g/mL a aproximadamente 0,79 g/mL, que es menor que la densidad del agua (1,0 g/mL).
Si hay un derrame de petróleo en el océano, los alcanos en el petróleo, que no se mezclan con el agua, forman una capa delgada en la superficie que se extiende sobre una gran área. En abril de 2010, una explosión en una plataforma de perforación de petróleo en el Golfo de México causó el mayor derrame de petróleo en la historia de EE. UU. En su máximo, se estima que se filtraron unos 10 millones de litros de petróleo cada día. Si el crudo llega a la tierra, puede causar un daño considerable a las playas, mariscos, aves y hábitats de vida silvestre. Cuando animales como las aves se cubren de petróleo, deben ser limpiados rápidamente porque la ingestión de hidrocarburos al intentar limpiarse es fatal.
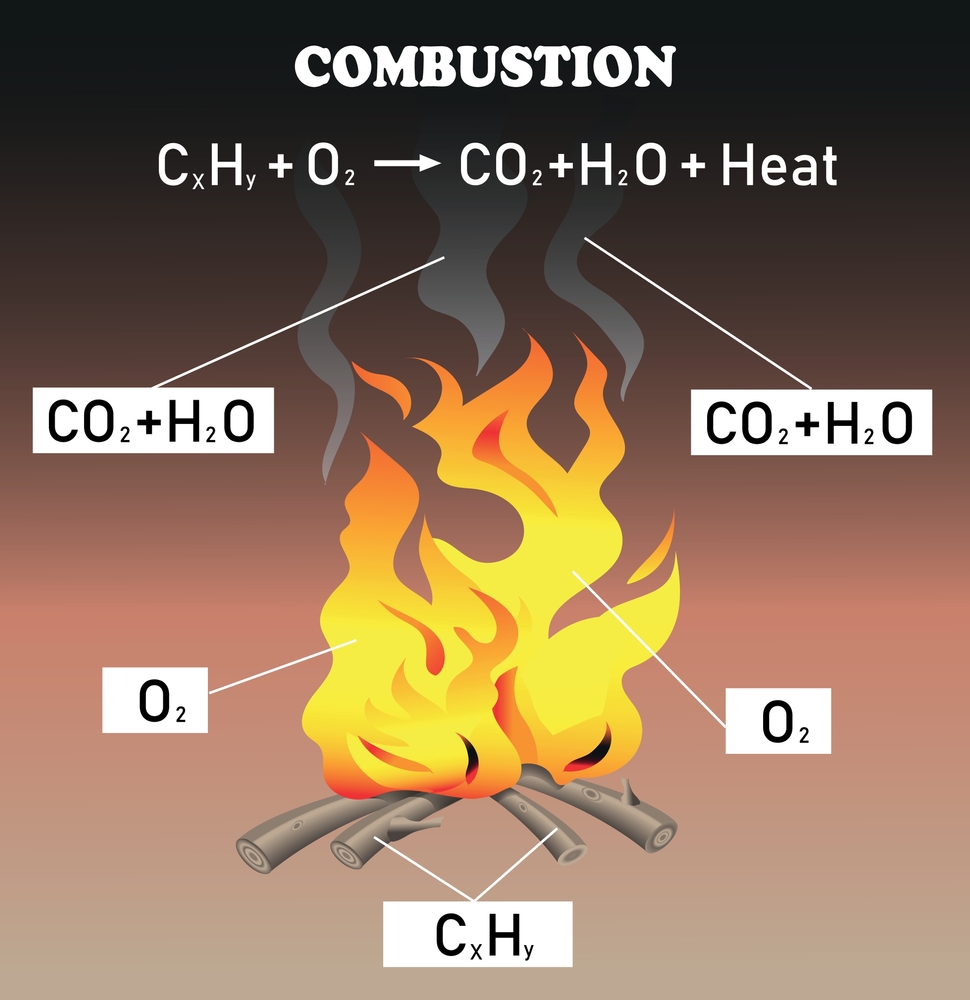
3. Combustión de alcanos
Los enlaces simples carbono-carbono en los alcanos son difíciles de romper, lo que los hace la familia menos reactiva de compuestos orgánicos. Sin embargo, los alcanos arden fácilmente en oxígeno para producir dióxido de carbono, agua y energía. Por ejemplo, el metano es el gas natural que usamos para cocinar nuestros alimentos en una estufa de gas y calentar nuestros hogares.
CH4 + 2O2 → CO2 + 2H2O + energía
El butano se utiliza en la cocina, el camping y las antorchas.
2C4H10 + 13O2 → 8CO2 + 10H2O + energía
Actividad: Ejercicios de práctica
1. Heptano, utilizado como solvente para cemento de caucho, tiene una densidad de 0,68 g/mL y hierve a 98 °C.
a) Dibuja las fórmulas estructural condensada y de líneas y ángulos para el heptano.
b) ¿Es el heptano un sólido, líquido o gas a temperatura ambiente?
c) ¿Es el heptano soluble en agua?
d) ¿El heptano flotará en el agua o se hundirá?
e) Escribe la ecuación química balanceada para la combustión completa del heptano.
2. Escribe la ecuación química balanceada para la combustión completa de los siguientes compuestos:
a) Etano
b) Ciclopropano
c) 2,3-dimetilhexano
