Los ésteres son una clase importante de compuestos orgánicos derivados de la reacción entre un ácido y un alcohol. Estos compuestos son ampliamente conocidos por sus aromas agradables y se encuentran en frutas, flores, y en numerosos productos industriales. Los ésteres tienen aplicaciones variadas, que van desde fragancias y sabores en la industria alimentaria hasta solventes en productos químicos.
Objetivo de aprendizaje
- Comprender y aplicar la estructura, propiedades y reacciones de los ésteres.
1. Definición y estructura química
Los ésteres son compuestos que se forman mediante la condensación de un ácido carboxílico y un alcohol, con la eliminación de una molécula de agua. La estructura general de un éster se puede representar como RCOOR’, donde R y R’ son grupos alquilo o arilo. El oxígeno doblemente enlazado a un carbono (grupo carbonilo) junto con otro oxígeno enlazado a un grupo R’ (grupo alcoxi) define la estructura de un éster.
2. Propiedades físicas
- Solubilidad: Los ésteres son generalmente solubles en solventes orgánicos y tienen una solubilidad limitada en agua debido a la capacidad del grupo ester para formar enlaces de hidrógeno con el agua, aunque menos efectivamente que los ácidos carboxílicos o alcoholes debido a la presencia del grupo alcoxi.
- Puntos de Ebullición: Los ésteres tienen puntos de ebullición más bajos que los ácidos carboxílicos correspondientes debido a la ausencia de un hidrógeno capaz de formar enlaces de hidrógeno intermoleculares fuertes como en los ácidos carboxílicos.
- Aroma: Muchos ésteres son volátiles y tienen aromas agradables y distintivos, razón por la cual son ingredientes comunes en fragancias y sabores artificiales.
3. Reactividad química
Los ésteres son relativamente estables, pero pueden participar en varias reacciones importantes:
- Hidrólisis: Los ésteres pueden ser hidrolizados en medios ácidos o básicos, regenerando el ácido carboxílico y el alcohol original. Esta reacción es fundamental en la digestión de grasas y en la fabricación industrial de jabones a partir de grasas y aceites.
- Saponificación: Es un caso especial de hidrólisis básica donde los ésteres de ácidos grasos reaccionan con una base fuerte para formar jabón y glicerina.
- Reacciones con Aminas: Los ésteres pueden reaccionar con aminas para formar amidas y alcoholes en un proceso conocido como transamidación.
4. Usos de los ésteres
- Industria Alimentaria y de Bebidas: Los ésteres son ampliamente utilizados como aditivos para impartir sabores y aromas a alimentos y bebidas. Por ejemplo, el acetato de isoamilo se usa para impartir un sabor a plátano.
- Fragancias y Cosméticos: Debido a sus agradables aromas, los ésteres se utilizan en la formulación de perfumes, colonias y productos cosméticos.
- Industria de los Plásticos: Algunos ésteres poliméricos, como el polietileno tereftalato (PET), son utilizados para fabricar envases de bebidas y textiles.
- Productos Farmacéuticos: Los ésteres también desempeñan un papel en la medicina, como solventes y como intermediarios en la síntesis de drogas.
- Solventes Industriales: Algunos ésteres se utilizan como solventes debido a su baja toxicidad y buena capacidad de disolución para ciertos compuestos orgánicos
5. Nomenclatura de ésteres
Regla 1. Los ésteres proceden de condensar ácidos con alcoholes y se nombran como sáles del ácido del que provienen. La nomenclatura IUPAC cambia la terminación -oico del ácido por -oato, terminando con el nombre del grupo alquilo unido al oxígeno.

Regla 2. Los esteres son grupos prioritarios frente a aminas, alcoholes, cetonas, aldehídos, nitrilos, amidas y haluros de alcanoilo. Estos grupos se nombran como sustituyentes siendo el éster el grupo funcional.

Regla 3. Ácidos carboxílicos y anhídridos tienen prioridad sobre los ésteres, que pasan a nombrarse como sustituyentes (alcoxicarbonil……)

Regla 4. Cuando el grupo éster va unido a un ciclo, se nombra el ciclo como cadena principal y se emplea la terminación -carboxilato de alquilo para nombrar el éster.

Ejercicios de práctica
1. Escriba la nomenclatura para las siguientes estructuras:
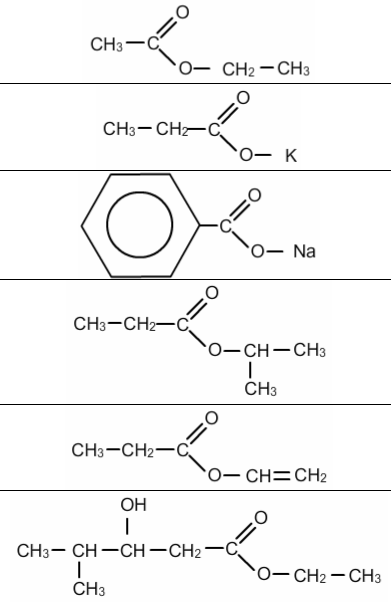
2. Represente las estructuras condensadas para los siguientes compuestos:
a) Propanoato de etilo
b) Butanoato de fenilo
c) 3-metilbutanoato de metilpropilo
d) 2-metil-3-pentenoato de isobutilo
e) 3-pentinoato de ciclobutilo
f) Benzoato de ciclohexilo
g) 3-carboxipentanodioato de etilo y metilo
h) Carboxidihidroxibutanoato de fenilo
i) m-formilbenzoato de etilo
j) 2-hidroxi-3-oxopentanoato de metilo
