Clasificación y características de las reacciones químicas

Destreza / Competencia:
CN.Q.5.1.14. Comparar los tipos de reacciones químicas: combinación, descomposición, desplazamiento, exotérmicas y endotérmicas, partiendo de la experimentación, análisis e interpretación de los datos registrados y la complementación de información bibliográfica y procedente de las TIC.

CN.Q.5.1.24. Interpretar y analizar las reacciones de oxidación y reducción como la transferencia de electrones que experimentan los elementos.
¿En qué áreas de la vida se puede aplicar este contenido?
El aprendizaje de estos contenidos te permite reconocer qué tipo de sustancia se está usando, cómo se comporta y qué precauciones requiere.
- Vida cotidiana: te ayudan a identificar compuestos presentes en sal de mesa, productos de limpieza, medicamentos, fertilizantes, baterías, alimentos y cosméticos, diferenciando si son óxidos, ácidos, bases o sales.
- Desarrollo personal: fortalecen tu capacidad de leer etiquetas, interpretar fórmulas químicas y usar sustancias con mayor seguridad, evitando mezclas peligrosas o usos incorrectos.
- Contexto social / académico: te permiten comprender procesos como neutralización, corrosión, contaminación, tratamiento de agua, fabricación de materiales y formulación química, base para estudiar reacciones químicas y estequiometría.
Anticipación
“¿Qué tipo de compuesto tengo?”
Muestra o menciona 5 sustancias cotidianas:
- sal de mesa
- vinagre
- cal
- cloro doméstico
- óxido de hierro
En parejas, responden:
- ¿Cuáles parecen ácidos, bases, sales u óxidos?
- ¿Qué pistas usaron para clasificarlos?
- ¿Por qué es importante saber qué tipo de compuesto estamos usando?
Luego conecta sus respuestas con la idea de que los compuestos químicos se clasifican según su composición, propiedades y comportamiento.
Construcción: tiempo
Introducción:
Toda reacción química somete a la materia a una transformación química, alterando su estructura y composición molecular (a diferencia de los cambios físicos que sólo afectan su forma o estado de agregación). Los cambios químicos generalmente producen sustancias nuevas, distintas de las que teníamos al principio.
Las reacciones químicas pueden darse de manera espontánea en la naturaleza (sin que intervenga el ser humano), o también pueden ser generadas por el ser humano en un laboratorio bajo condiciones controladas.
Características de una reacción química Las reacciones químicas se caracterizan por los siguientes aspectos:
Irreversibilidad.
Las reacciones químicas son procesos irreversibles, es decir, involucran la formación o destrucción de enlaces químicos entre las moléculas de los reactivos, generando una pérdida o ganancia de energía.
Transformación de materia.
En una reacción química, la materia se transforma profundamente, aunque en ocasiones esta recomposición no pueda apreciarse a simple vista.
Medición precisa.
Las proporciones de los reactivos pueden medirse, de lo cual se ocupa la estequiometría, rama encargada de las relaciones cuantitativas en las reacciones químicas.
Productos variables.
Las reacciones químicas generan productos que pueden variar dependiendo de la naturaleza de los reactivos, pero también de las condiciones en que la reacción se produzca.
Velocidad controlable.
La velocidad en las reacciones químicas es importante, ya que el control de la velocidad es fundamental para su empleo en la industria, la medicina, etc. Además, existen métodos para aumentar o disminuir la velocidad de una reacción química. Para ello, se emplean los catalizadores, que no intervienen en las reacciones, solo controlan la velocidad a la que ocurren. Asimismo, existen los inhibidores, que, por el contrario, disminuyen la velocidad.
¿Cómo se representa una reacción química?
Las reacciones químicas se representan mediante ecuaciones químicas, es decir, fórmulas en las que se describen los reactivos participantes y los productos obtenidos, a menudo indicando determinadas condiciones propias de la reacción, como la presencia de calor, catalizadores, luz etc.
La primera ecuación química de la historia fue redactada en 1615 por Jean Beguin, en uno de los primeros tratados sobre química, el Tyrocinium Chymicum. Hoy son de enseñanza común y gracias a ellas podemos visualizar con mayor facilidad lo que está ocurriendo en una reacción determinada.
La forma general de representar una ecuación química es:
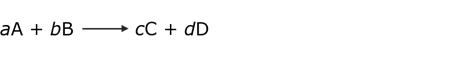
Donde:
- A y B son los reactivos.
- C y D son los productos.
- a, b, c y d son los coeficientes estequiométricos (son números que indican la cantidad de reactivos y productos) que deben ser ajustados de manera que haya la misma cantidad de cada elemento en los reactivos y en los productos. De esta forma se cumple la Ley de Conservación de la Masa (que establece que la masa no se crea ni se destruye, solo se transforma).
En una reacción química los átomos se reacomodan formando nuevas sustancias.
Símbolos utilizados
Para representar las reacciones químicas mediante ecuaciones, es importante emplear un conjunto de símbolos:
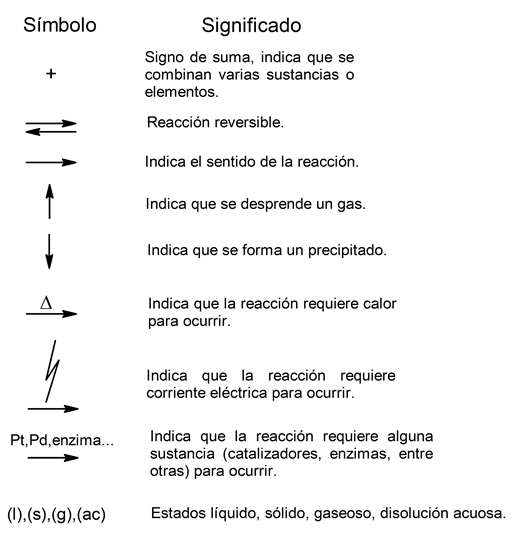
Tipos de reacciones químicas y ejemplos
Las reacciones químicas pueden clasificarse según el tipo de reactivos que reaccionan. Con base en esto, se pueden distinguir reacciones químicas inorgánicas y reacciones químicas orgánicas. En este capítulo nos vamos a centrar en las REACCIONES QUÍMICAS INORGÁNICAS, y revisaremos los diferentes criterios que se tienen para clasificarlas:
Utilizamos el siguiente recurso interactivo para revisar la clasificación de las reacciones químicas:
Clasificación de las reacciones químicas
Toca cada tarjeta para ver la subclasificación
Según el tipo de transformación
4 tipos
↻- Síntesis o adición
- Descomposición
- Sustitución simple
- Sustitución doble
Según el tipo y forma de energía
6 tipos
↻- Endotérmicas
- Exotérmicas
- Endoluminosas
- Exoluminosas
- Endoeléctricas
- Exoeléctricas
Según la velocidad de reacción
2 tipos
↻- Reacciones lentas
- Reacciones rápidas
Según el tipo de partícula involucrada
2 tipos
↻- Reacciones ácido-base
- Reacciones de oxidación-reducción
Según el sentido de la reacción
2 tipos
↻- Reacciones reversibles
- Reacciones irreversibles
A continuación, encontrarás información detallada y ejemplos de cada subclasificación de las reacciones químicas:
Según el tipo de transformación:
Reacciones de síntesis o adición.
Dos sustancias se combinan para dar como resultado una sustancia diferente. Por ejemplo:
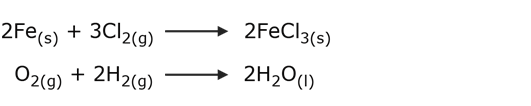
Reacciones de descomposición.
Una sustancia se descompone en sus componentes simples, o una sustancia reacciona con otra y se descompone en otras sustancias que contienen los componentes de esta. Por ejemplo:
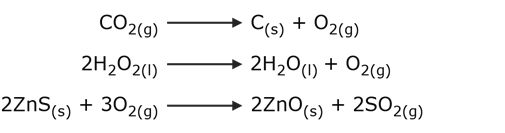
Reacciones de desplazamiento o sustitución simple.
Un compuesto o elemento ocupa el lugar de otro en un compuesto, sustituyéndolo y dejándolo libre. Por ejemplo:

Reacciones de sustitución doble.
Dos reactivos intercambian compuestos o elementos químicos simultáneamente. Por ejemplo:
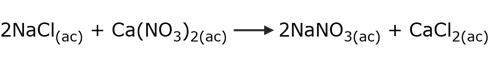
Según el tipo y la forma de la energía intercambiada
Reacciones endotérmicas
Se absorbe calor para que la reacción pueda ocurrir. Por ejemplo:

Reacciones exotérmicas
Se desprende calor cuando la reacción ocurre. Por ejemplo:
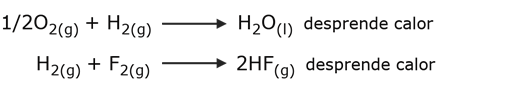
Reacciones endoluminosas
Se necesita luz para que ocurra la reacción. Por ejemplo: la fotosíntesis.

Reacciones exoluminosas
Se desprende luz cuando ocurre la reacción. Por ejemplo:

Reacciones endoeléctricas
Se necesita energía eléctrica para que la reacción ocurra. Por ejemplo:
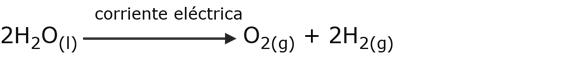
Reacciones exoeléctricas
Se desprende o se genera energía eléctrica cuando ocurre la reacción. Por ejemplo:
Según la velocidad de reacción:
Reacciones lentas
La cantidad de reactivos consumidos y la cantidad de productos formados en un tiempo determinado es muy poca. Por ejemplo: la oxidación del hierro. Es una reacción lenta, que vemos cotidianamente en los objetos de hierro que están oxidados. Si no fuese lenta esta reacción, no tendríamos estructuras de hierro muy antiguas en el mundo actual.

Reacciones rápidas
La cantidad de reactivos consumidos y la cantidad de productos formados en un tiempo determinado es mucha. Por ejemplo: la reacción del sodio con el agua es una reacción que además de ocurrir rápidamente es muy peligrosa.

Según el tipo de partícula involucrada:
Reacciones ácido-base
Se transfieren protones (H+). Por ejemplo:

Reacciones de oxidación-reducción
Se transfieren electrones. En este tipo de reacción debemos fijarnos en el número de oxidación de los elementos involucrados. Si el número de oxidación de un elemento aumenta, este se oxida, si disminuye, este se reduce. Por ejemplo: en esta reacción se oxida el hierro y se reduce el cobalto.

Según el sentido de la reacción:
Reacciones reversibles
Se dan en ambos sentidos, es decir, los productos pueden volver a convertirse en los reactivos. Por ejemplo:

Reacciones irreversibles
Se dan en un solo sentido, es decir, los reactivos se transforman en productos y no puede ocurrir el proceso contrario. Por ejemplo:

Velocidad de una reacción química
Las reacciones químicas requieren de un tiempo estipulado para suceder, el cual varía dependiendo de la naturaleza de los reactivos y del entorno en el que la reacción se produzca.
Los factores que afectan la velocidad de las reacciones químicas por lo general suelen ser:
Aumento de oT
Las altas temperaturas tienden a aumentar la velocidad de las reacciones químicas.
Aumento de P
Al aumentar la presión se suele aumentar la velocidad de las reacciones químicas. Esto ocurre generalmente cuando reaccionan sustancias que son sensibles a los cambios de presión, como son los gases. En el caso de líquidos y sólidos, los cambios de presión no provocan cambios importantes en la velocidad de sus reacciones.
Estado de agregación de los reactivos
Los sólidos suelen reaccionar más lentamente que los líquidos o los gases, aunque la velocidad también dependerá de la reactividad de cada sustancia.
Presencia de catalizadores
Estas sustancias no intervienen en las reacciones, solo controlan la velocidad a la que ocurren. También existen sustancias llamadas inhibidores, que se emplean de la misma forma pero provocan el efecto contrario, es decir, disminuyen la velocidad de las reacciones.
Energía luminosa
Algunas reacciones químicas son aceleradas cuando se les hace incidir luz.
Concentración de los reactivos
La mayoría de las reacciones químicas ocurren más rápido si tienen una alta concentración de sus reactivos.
Consolidación:
Se consolidará este tema mediante el desarrollo de la práctica de laboratorio sugerida.
Sugerencia Rúbrica
RÚBRICA: Informe de prácticas de laboratorio
https://docs.google.com/spreadsheets/d/1AWYMzSl6BPYz6TqUBBPIPP3pYw_eSEPDg9uTExkgh7s/edit?gid=0#gid=0
Práctica de laboratorio sugerida:
PRÁCTICA DE LABORATORIO #4: OBSERVACIÓN DE REACCIONES REDOX CON COMPORTAMIENTO OSCILANTE
Llevamos a cabo el desarrollo de reacciones químicas en donde podremos realizar la observación de reacciones redox que presetnan un comportamiento oscilante o reversible.
Nos basamos en las instrucciones dadas en la GUÍA DE PRACTICAS DE LABORATORIO que está adjunta al QUIMIOKIT, y observamos el siguiente material audiovisual para seguir sus instrucciones:
Después de haber desarrollado los experimentos, elaboramos el informe correspondiente (en la guía de prácticas de laboratorio), lo revisamos y calificamos con la RÚBRICA DE INFORMES DE PRÁCTICAS DE LABORATORIO, la misma que fue socializada anteriormente y facilitada a los alumnos en Classroom.
NEE – Agregar el tipo de adaptaciones curriculares
Principio II: Pautas 6.1 – 6.3 – 6.4
Principio III: Pautas 7.1 – 8.1 – 9.1
ALUMNO 1: Constante monitoreo. Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 2: Constante monitoreo, Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 3: Constante monitoreo. Corroborar que el contenido entregado en clase haya sido comprendido por la estudiante mediante retroalimentación.
