
Destreza / Competencia:
CN.Q.5.2.9. Experimentar y deducir el cumplimiento de las leyes de transformación de la materia: leyes ponderales y de la conservación de la materia que rigen la formación de compuestos químicos.

CN.Q.5.1.26. Aplicar y experimentar diferentes métodos de igualación de ecuaciones tomando en cuenta el cumplimiento de la ley de la conservación de la masa y la energía, así como las reglas de número de oxidación en la igualación de las ecuaciones de óxido-reducción.

¿En qué áreas de la vida se puede aplicar este contenido?
Estos contenidos te permiten calcular cantidades exactas de reactivos y productos, evitando desperdicios, errores y riesgos.
- Vida cotidiana: te ayudan a comprender proporciones en productos como medicamentos, fertilizantes, alimentos, combustibles y soluciones de limpieza, donde usar cantidades correctas es importante.
- Desarrollo personal: fortalecen tu capacidad de hacer cálculos precisos, interpretar datos y entender que en una reacción química la materia se conserva: nada aparece ni desaparece, solo se transforma.
- Contexto social / académico: te permiten resolver problemas de laboratorio, calcular reactivos, identificar el reactivo limitante, estimar rendimiento y comprender procesos industriales, ambientales, farmacéuticos y alimentarios.
Actividades de aprendizaje
Anticipación
“La receta química”
Presenta esta comparación:
“Si para hacer 1 sánduche necesitas 2 panes y 1 queso, ¿cuántos sánduches puedes hacer con 10 panes y 3 quesos?”
Pregunta:
- ¿Qué ingrediente se acaba primero?
- ¿Cuál sobra?
- ¿Cómo sabes cuántos productos puedes formar?
- ¿Qué pasaría si no respetas las proporciones?
Cierra explicando que en química ocurre algo similar: las reacciones necesitan proporciones exactas, y la estequiometría permite calcular reactivos, productos, excesos y límites.
Construcción:
ETIMOLOGÍA DE LA ESTEQUIOMETRÍA:
Lo primero que vamos a hacer es conocer el origen etimológico del término estequiometría. En concreto, tenemos que establecer que se trata de un neologismo que deriva del griego pues es fruto de la suma de tres componentes léxicos de dicha lengua como son estos:
-La palabra “stoicheion”, que se utiliza para hacer referencia a un elemento básico que forma parte de una serie que está ordenada.
-El sustantivo “metron”, que es sinónimo de “medida”.
-El sufijo “-ia”, que indica “cualidad”.
En nuestro idioma el término se convirtió en estequiometría, una idea que se utiliza en el ámbito de la química.
CONCEPTOS IMPORTANTES:
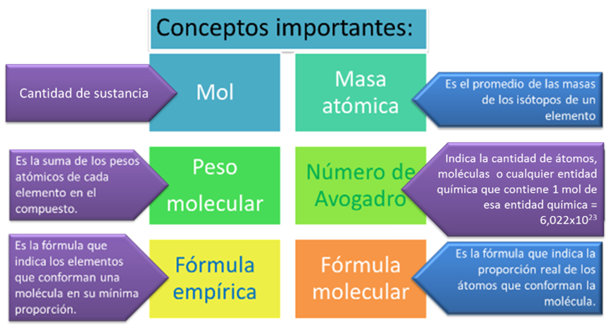
PRINCIPIOS BÁSICOS DE LA ESTEQUIOMETRÍA EN QUÍMICA
La estequiometría es la rama de la química que estudia las relaciones cuantitativas entre los reactivos y los productos en una reacción química. Permite responder preguntas como: ¿cuánta sustancia se necesita?, ¿cuánto producto se forma? y ¿qué reactivo se consume primero?
LEY DE CONSERVACIÓN DE LA MASA
Definición
La Ley de Conservación de la Masa, propuesta por Antoine Lavoisier, establece que:
“La materia no se crea ni se destruye, solo se transforma”.
Esto significa que en una reacción química:
- la masa total de los reactivos es igual a la masa total de los productos,
- los átomos no desaparecen ni se generan nuevos,
- simplemente se reorganizan.
Ejemplo:
2H₂ + O₂ → 2H₂O
Antes de la reacción:
- 4 átomos de H
- 2 átomos de O
Después de la reacción:
- 4 átomos de H
- 2 átomos de O
Se conserva el número de átomos y, por tanto, la masa.
APLICACIÓN DE LA LEY EN LA ESTEQUIOMETRÍA
Uso de ecuaciones químicas balanceadas
Las ecuaciones químicas deben estar balanceadas para cumplir la ley de conservación de la masa. Esto asegura que:
- el número de átomos de cada elemento sea igual en ambos lados,
- las proporciones entre sustancias sean correctas.
Ejemplo:
N₂ + 3H₂ → 2NH₃
Aquí, los coeficientes indican la proporción en la que reaccionan las sustancias.
Relación molar
Los coeficientes de una ecuación balanceada representan relaciones en moles.
Ejemplo:
En la reacción anterior:
- 1 mol de N₂ reacciona con 3 moles de H₂
- se producen 2 moles de NH₃
Unidades en estequiometría
Los cálculos pueden expresarse en:
- moles (unidad base en química),
- gramos (usando masa molar),
- partículas (usando el número de Avogadro: 6,022 × 10²³).
IMPORTANCIA DE LA ESTEQUIOMETRÍA
La estequiometría permite:
- predecir cantidades de productos,
- optimizar el uso de reactivos,
- reducir desperdicios,
- controlar procesos químicos,
- interpretar resultados experimentales.
REACTIVO LIMITANTE
Definición
El reactivo limitante es el reactivo que se consume completamente primero y, por tanto, determina la cantidad máxima de producto que se puede formar.
El otro reactivo se denomina reactivo en exceso.
Cómo identificarlo
Se comparan las cantidades disponibles de reactivos con las proporciones de la ecuación balanceada.
El que produce menor cantidad de producto es el reactivo limitante.
Uso del exceso de reactivos
En muchos procesos se utiliza un reactivo en exceso para asegurar que el reactivo limitante reaccione completamente.
COMPOSICIÓN PORCENTUAL
La composición porcentual indica qué porcentaje de una mezcla o compuesto corresponde a cada sustancia.
Fórmula:
% = (masa del componente / masa total) × 100
Permite:
- analizar la pureza,
- caracterizar mezclas,
- controlar calidad en procesos químicos.
RENDIMIENTO DE UNA REACCIÓN
Rendimiento teórico
Es la cantidad máxima de producto que se puede obtener según los cálculos estequiométricos.
Rendimiento real
Es la cantidad de producto que realmente se obtiene en el laboratorio o industria.
Factores que afectan el rendimiento real
- pérdidas de material,
- reacciones secundarias,
- impurezas,
- errores experimentales,
- condiciones no ideales.
Rendimiento porcentual
Fórmula:
% rendimiento = (rendimiento real / rendimiento teórico) × 100
Indica la eficiencia de la reacción.
Consolidación:
AGC: “DETECTIVES DE LA REACCIÓN”
Objetivo:
Consolidar los conceptos de ley de conservación de la masa, reactivo limitante, rendimiento teórico y rendimiento real.
Materiales:
Hoja de trabajo, calculadora y tabla periódica.
Instrucciones:
Forma equipos de 3 o 4 estudiantes. Entrega a cada grupo el siguiente caso:
Caso:
Se hacen reaccionar 4 g de hidrógeno (H₂) con 32 g de oxígeno (O₂) para formar agua.
Ecuación balanceada:
2H₂ + O₂ → 2H₂O
Parte 1. Conservación de la masa
- Calculen la masa total de los reactivos.
- Predigan la masa total de los productos según la ley de conservación de la masa.
- Expliquen por qué esa masa debe conservarse.
Parte 2. Reactivo limitante
- Determinen cuántos moles de H₂ y O₂ hay.
- Identifiquen cuál es el reactivo limitante.
- Expliquen por qué el otro reactivo está en exceso.
Parte 3. Rendimiento
- Calculen la cantidad teórica de agua que debería formarse.
- Si en el experimento se obtuvieron 30 g de agua, calculen el rendimiento porcentual.
- Propongan dos razones por las que el rendimiento real fue menor al teórico.
Parte 4. Cierre reflexivo
- Escriban en 3 líneas qué relación existe entre:
- ley de conservación de la masa,
- ecuación balanceada,
- reactivo limitante,
- rendimiento experimental.
Cierre en clase:
Cada grupo comparte una respuesta clave. Luego se corrige en plenaria, reforzando que:
- la masa se conserva,
- el reactivo limitante determina cuánto producto se forma,
- el rendimiento real casi nunca coincide exactamente con el teórico.
Sugerencia Rúbrica
RÚBRICA: Banco de ejercicios.
https://docs.google.com/spreadsheets/d/1AWYMzSl6BPYz6TqUBBPIPP3pYw_eSEPDg9uTExkgh7s/edit?gid=0#gid=0
NEE – Agregar el tipo de adaptaciones curriculares
Principio II: Pautas 6.1 – 6.3 – 6.4
Principio III: Pautas 7.1 – 8.1 – 9.1
ALUMNO 1: Constante monitoreo. Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 2: Constante monitoreo, Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 3: Constante monitoreo. Corroborar que el contenido entregado en clase haya sido comprendido por la estudiante mediante retroalimentación.
