Destreza / Competencia:
CN.Q.5.1.5. Observar y aplicar el modelo mecánico-cuántico de la materia en la estructuración de la configuración electrónica de los átomos considerando la dualidad del electrón, los números cuánticos, los tipos de orbitales y la regla e Hund.

¿En qué áreas de la vida se puede aplicar este contenido?
Este contenido te permiten entender cómo se distribuyen los electrones en los átomos y, a partir de eso, explicar por qué los elementos reaccionan, se unen o tienen propiedades distintas.
- Vida cotidiana: te ayudan a comprender por qué ciertos elementos se usan en baterías, focos, cables, pantallas, medicamentos y materiales de uso diario, según la forma en que sus electrones están organizados.
- Desarrollo personal: fortalecen tu capacidad de relacionar la estructura interna de la materia con sus propiedades, entendiendo por qué algunos átomos son más reactivos que otros o por qué forman ciertos compuestos.
- Contexto social / académico: te permiten interpretar mejor temas como tabla periódica, enlaces químicos, formación de compuestos, reactividad y propiedades periódicas, que son base para estudios posteriores en química, salud, ingeniería y tecnología.
Actividades de aprendizaje:
Anticipación
“¿Por qué no todos los átomos se comportan igual?”
Escribe en la pizarra los nombres de algunos elementos conocidos, por ejemplo: sodio, oxígeno, calcio, cloro y neón. Luego pregúntales:
- ¿Por qué algunos elementos reaccionan fácilmente y otros casi no reaccionan?
- ¿Por qué unos forman sales, otros gases y otros metales?
- ¿Qué tendrá que ver esto con la manera en que están acomodados sus electrones?
Después conecta sus respuestas explicando que la configuración electrónica permite entender cómo están distribuidos los electrones en un átomo y por qué eso determina su comportamiento químico.
Construcción: tiempo
Configuración electrónica: Fundamentos y significado
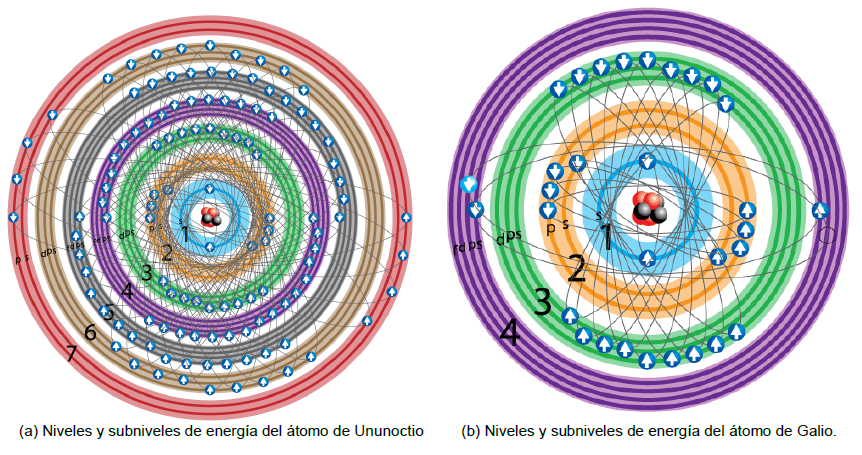
La configuración electrónica es la representación de la distribución de los electrones en los orbitales atómicos de un elemento. Esta distribución es clave para comprender las propiedades químicas y físicas de los elementos, ya que determina la forma en que los electrones interactúan con otros átomos. Los electrones se organizan en orbitales siguiendo el principio de mínima energía, ocupando primero los orbitales de menor energía. El orden de llenado se basa en los números cuánticos principal (n) y azimutal (l), siguiendo el diagrama de Moeller o la regla de las diagonales para determinar la secuencia de llenado.
Jerarquía energética de orbitales y el Principio de Exclusión de Pauli
La energía de los orbitales atómicos se define por los números cuánticos n y l, lo que da lugar a una jerarquía energética dentro de los niveles electrónicos. Los orbitales con igual energía se conocen como degenerados, como es el caso de los tres orbitales p (px, py, pz). El principio de exclusión de Pauli es una regla fundamental que prohíbe la coexistencia de dos electrones con idénticos números cuánticos en un mismo átomo, lo que implica que cada orbital puede albergar como máximo dos electrones con espines opuestos.
Principio de Aufbau y la Regla de Hund
El principio de Aufbau, o de construcción, establece que el llenado de los orbitales atómicos por electrones se realiza de manera secuencial, empezando por los de menor energía. Este principio se complementa con la regla de máxima multiplicidad de Hund, que indica que los electrones se distribuyen primero en orbitales degenerados sin emparejar sus espines, maximizando así el número de espines paralelos. La notación simplificada de la configuración electrónica utiliza el símbolo del gas noble más cercano en la tabla periódica, seguido de la descripción de los electrones en los orbitales restantes.
DIAGRAMA DE MöELLER:
El diagrama de Möller surgió como una herramienta gráfica y nemotécnica para representar de forma sencilla el orden de llenado de los orbitales en la configuración electrónica. Su base teórica está en varias reglas y principios, según los cuales los electrones van ocupando primero los orbitales de menor energía y luego los de mayor energía:
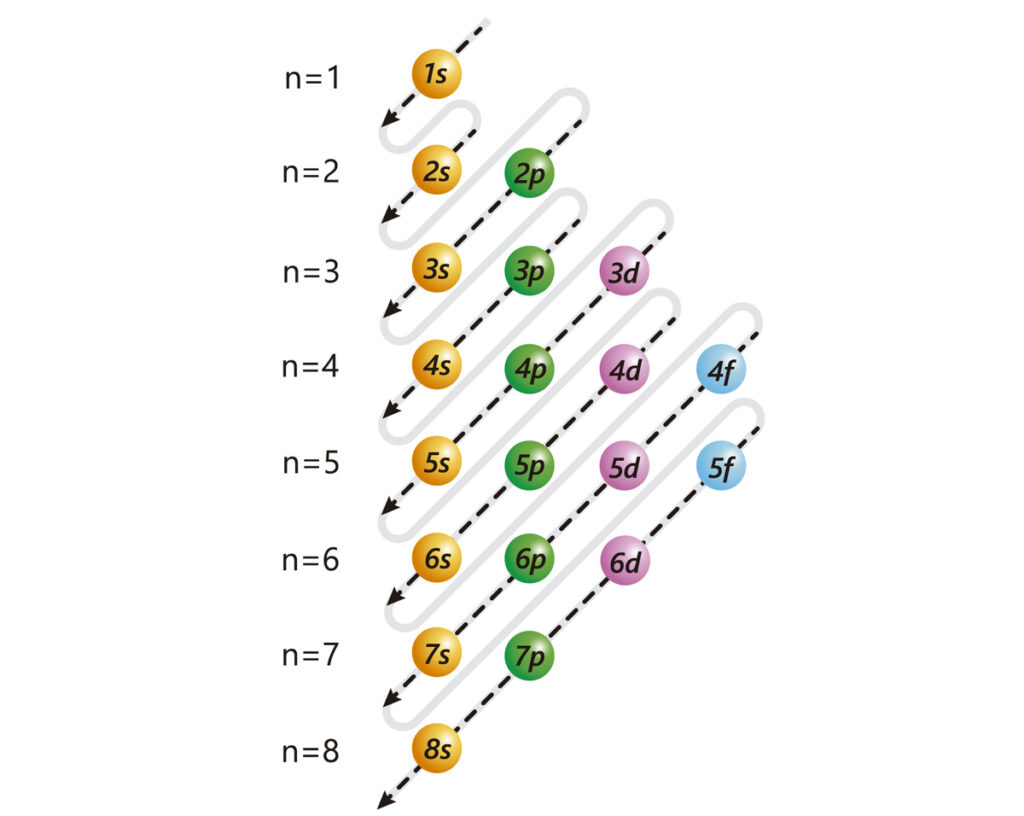
Vamos a observar este video para aprender cómo se va llenando este diagrama con los electrones de los átomos de un elemento químico. Recuerda siempre tener contigo la tabla periódica, para poder cotejar la información que ella nos brinda:
EJERCICIO RESUELTO
Capacidad máxima de cada subnivel:
s = 2 electrones
p = 6 electrones
d = 10 electrones
f = 14 electrones
Pasos para realizar la configuración electrónica:
- Identificar el número atómico del elemento.
- Determinar el número total de electrones.
- Seguir el orden de llenado del diagrama de Möller.
- Distribuir los electrones respetando la capacidad de cada subnivel.
- Verificar que la suma total coincida con el número atómico.
APLICACIÓN:
Aluminio (Al) — Z = 13
Tiene 13 electrones.
Configuración electrónica:
1s² 2s² 2p⁶ 3s² 3p¹
Comprobación:
2 + 2 + 6 + 2 + 1 = 13
Consolidación:
AIC: VAMOS A REALIZAR LA CONFIGURACIÓN ELECTRÓNICA CON EL DIAGRAMA DE MÖLLER
- Sodio (Na) — Z = 11
Tiene 11 electrones.
Configuración electrónica:
1s² 2s² 2p⁶ 3s¹
Comprobación:
2 + 2 + 6 + 1 = 11
- Oxígeno (O) — Z = 8
Tiene 8 electrones.
Configuración electrónica:
1s² 2s² 2p⁴
Comprobación:
2 + 2 + 4 = 8
- Calcio (Ca) — Z = 20
Tiene 20 electrones.
Configuración electrónica:
1s² 2s² 2p⁶ 3s² 3p⁶ 4s²
Comprobación:
2 + 2 + 6 + 2 + 6 + 2 = 20
- Cloro (Cl) — Z = 17
Tiene 17 electrones.
Configuración electrónica:
1s² 2s² 2p⁶ 3s² 3p⁵
Comprobación:
2 + 2 + 6 + 2 + 5 = 17
- Magnesio (Mg) — Z = 12
Tiene 12 electrones.
Configuración electrónica:
1s² 2s² 2p⁶ 3s²
Comprobación:
2 + 2 + 6 + 2 = 12
Sugerencia Rúbrica
RÚBRICA: Banco de ejercicios
https://docs.google.com/spreadsheets/d/1AWYMzSl6BPYz6TqUBBPIPP3pYw_eSEPDg9uTExkgh7s/edit?gid=0#gid=0
PRÁCTICA DE LABORATORIO SUGERIDA:
PRÁCTICA DE LABORATORIO #3: OBTENCIÓN EXPERIMENTAL DE HIDRÓGENO
Llevamos a cabo el desarrollo de la obtención experimental del elemento hidrógeno, observando algunas de sus propiedades físico-químicas.
Nos basamos en las instrucciones dadas en la GUÍA DE PRACTICAS DE LABORATORIO que está adjunta al QUIMIOKIT, y observamos el siguiente material audiovisual para seguir sus instrucciones:
Después de haber desarrollado los experimentos, elaboramos el informe correspondiente (en la guía de prácticas de laboratorio), lo revisamos y calificamos con la RÚBRICA DE INFORMES DE PRÁCTICAS DE LABORATORIO, la misma que fue socializada anteriormente y facilitada a los alumnos en Classroom.
NEE – Agregar el tipo de adaptaciones curriculares
Principio II: Pautas 6.1 – 6.3 – 6.4
Principio III: Pautas 7.1 – 8.1 – 9.1
ALUMNO 1: Constante monitoreo. Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 2: Constante monitoreo, Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 3: Constante monitoreo. Corroborar que el contenido entregado en clase haya sido comprendido por la estudiante mediante retroalimentación.
