
Destreza / Competencia:
CN. Q.5.1.12: Deducir y predecir la posibilidad de formación de compuestos químicos, con base en el estado natural de los elementos, su estructura electrónica y su ubicación en la tabla periódica.
CN.Q.5.1.11. Establecer y diferenciar las fuerzas intermoleculares partiendo de la descripción del puente de hidrógeno, fuerzas de London y de Van der Walls, y dipolo-dipolo.
¿En qué áreas de la vida se puede aplicar este contenido?
Te ayuda a entender y controlar procesos donde la materia cambia de estado por temperatura o presión, sin cambiar su composición, para usar energía y materiales de forma segura y eficiente.
- Vida cotidiana: cocinas y conservas mejor (hervir, congelar, derretir, evaporar, condensación en tapas/ventanas), ajustando tiempos y temperaturas para resultados consistentes.
- Desarrollo personal: tomas decisiones de cuidado y seguridad (quemaduras por vapor vs agua, uso correcto de refrigeración, manejo de aerosoles y gases), entendiendo qué cambios son físicos y reversibles.
- Contexto social / académico: interpretas fenómenos y tecnologías (ciclo del agua, refrigeradores y aires acondicionados, destilación, licuefacción de gases), relacionando estado–cambio–energía (absorbe/libera calor).
ACTIVIDADES DE APRENDIZAJE:
Anticipación
Muestra 6 situaciones rápidas (en texto, video o imágenes): hielo derritiéndose, agua hirviendo, vapor en un espejo (condensación), ropa secándose, escarcha en el congelador, naftalina “desapareciendo”.
En parejas (3 min) deben: nombrar el cambio (fusión, ebullición, condensación, evaporación, solidificación, sublimación) y decir si absorbe o libera calor.
Con 2–3 respuestas del grupo tendremos una introducción a estados y cambios físicos.
Construcción
Para poder comprender por qué se dan los estados de agregación de la materia tal y como los conocemos, y por qué cada uno tiene sus características específicas, vamos a aprender sobre las fuerzas que los determinan:
Las fuerzas intermoleculares son interacciones de cohesión o de repulsión que actúan entre moléculas, determinando propiedades físicas como puntos de fusión, ebullición y estado de agregación. La cohesión une moléculas (atracción), mientras que las fuerzas de repulsión las mantienen separadas, predominando una u otra según la energía cinética y proximidad. En todos los estados de la materia, estas fuerzas coexisten simultáneamente.
Fuerzas de cohesión:
Mantienen las moléculas unidas, siendo predominantes en sólidos (forma definida, incompresibles) y fuertes en líquidos (tensión superficial). Ejemplos clave son los enlaces de hidrógeno y las fuerzas de Van der Waals (dipolo-dipolo, London).
Fuerzas de repulsión:
Se generan cuando las moléculas están demasiado cerca, dominando en el estado gaseoso, lo que resulta en alta compresibilidad y expansión.
Balance molecular:
El estado de la materia depende del equilibrio entre atracción y repulsión; a mayor temperatura, mayor energía cinética, lo que debilita la cohesión y aumenta la repulsión, facilitando la evaporación.
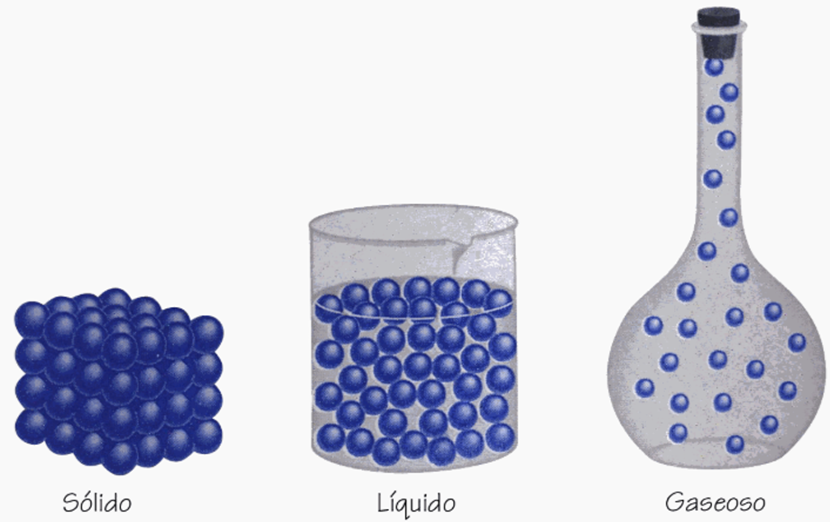
Vamos a aprender más sobre los estados de la materia con el siguiente recurso interactivo:
https://cards.algoreducation.com/es/content/a71oqlHa/estados-materia-caracteristicas
Consolidación:
AIC: Después de haber revisado el contenido propuesto, vamos a resolver las siguientes preguntas:
¿Cuáles son las características distintivas de los cuatro estados fundamentales de la materia?
¿Cómo explica la teoría cinética de la materia el comportamiento de los distintos estados?
¿Qué son los cambios de estado y cuáles son los procesos principales?
¿Cómo se diferencian las sustancias puras de las mezclas?
¿Qué tipos de mezclas existen y cómo se pueden distinguir?
Sugerencia Rúbrica
RÚBRICA de resumenes
https://docs.google.com/spreadsheets/d/1AWYMzSl6BPYz6TqUBBPIPP3pYw_eSEPDg9uTExkgh7s/edit?gid=0#gid=0
NEE – Agregar el tipo de adaptaciones curriculares
Principio II: Pautas 6.1 – 6.3 – 6.4
Principio III: Pautas 7.1 – 8.1 – 9.1
ALUMNO 1: Constante monitoreo. Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 2: Constante monitoreo, Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 3: Constante monitoreo. Corroborar que el contenido entregado en clase haya sido comprendido por la estudiante mediante retroalimentación.
