
Destreza:
| CN.Q.5.1.5. Observar y aplicar el modelo mecánico-cuántico de la materia en la estructuración de la configuración electrónica de los átomos considerando la dualidad del electrón, los números cuánticos, los tipos de orbitales y la regla de Hund. |
¿En qué áreas de la vida se puede aplicar este contenido?
Este contenido te permite entender cómo están organizados los electrones en los átomos, y eso explica muchas propiedades de los materiales y sustancias que usamos a diario.
- Vida cotidiana: te ayudan a comprender por qué algunos elementos conducen electricidad, otros forman imanes, y otros se usan en pantallas, baterías, focos LED y dispositivos electrónicos.
- Desarrollo personal: fortalecen tu capacidad de interpretar cómo la ciencia explica lo invisible, relacionando la estructura del átomo con el comportamiento de la materia.
- Contexto social / académico: te permiten entender mejor temas como la tabla periódica, los enlaces químicos, la configuración electrónica y la formación de compuestos, que son base para estudiar química, física, medicina, ingeniería y tecnología.
Anticipación
“La dirección del electrón”
Diles a tus alumnos que imaginen un edificio enorme donde viven millones de personas. Luego pregúntales:
- ¿Basta con decir solo el nombre de una persona para encontrarla?
- ¿Qué datos adicionales necesitarías?
- ¿Piso, número de departamento, ubicación y orientación podrían ayudarte?
Después conecta sus respuestas con la idea de que, en el átomo, los electrones también necesitan una especie de “dirección” para ubicarlos con precisión. Explica que esa “dirección” la dan los números cuánticos, porque indican nivel de energía, subnivel, orbital y espín.
Construcción: tiempo
NÚMEROS CUÁNTICOS
Los números cuánticos son valores que permiten describir la posición y el comportamiento de un electrón dentro del átomo. Gracias a ellos, podemos identificar en qué nivel de energía se encuentra, en qué subnivel, en qué orbital y cuál es el sentido de su giro.
Los números cuánticos permiten describir con precisión la ubicación y comportamiento de los electrones, lo que ayuda a entender la estructura del átomo y sus propiedades químicas. Cada electrón está definido por cuatro números cuánticos:
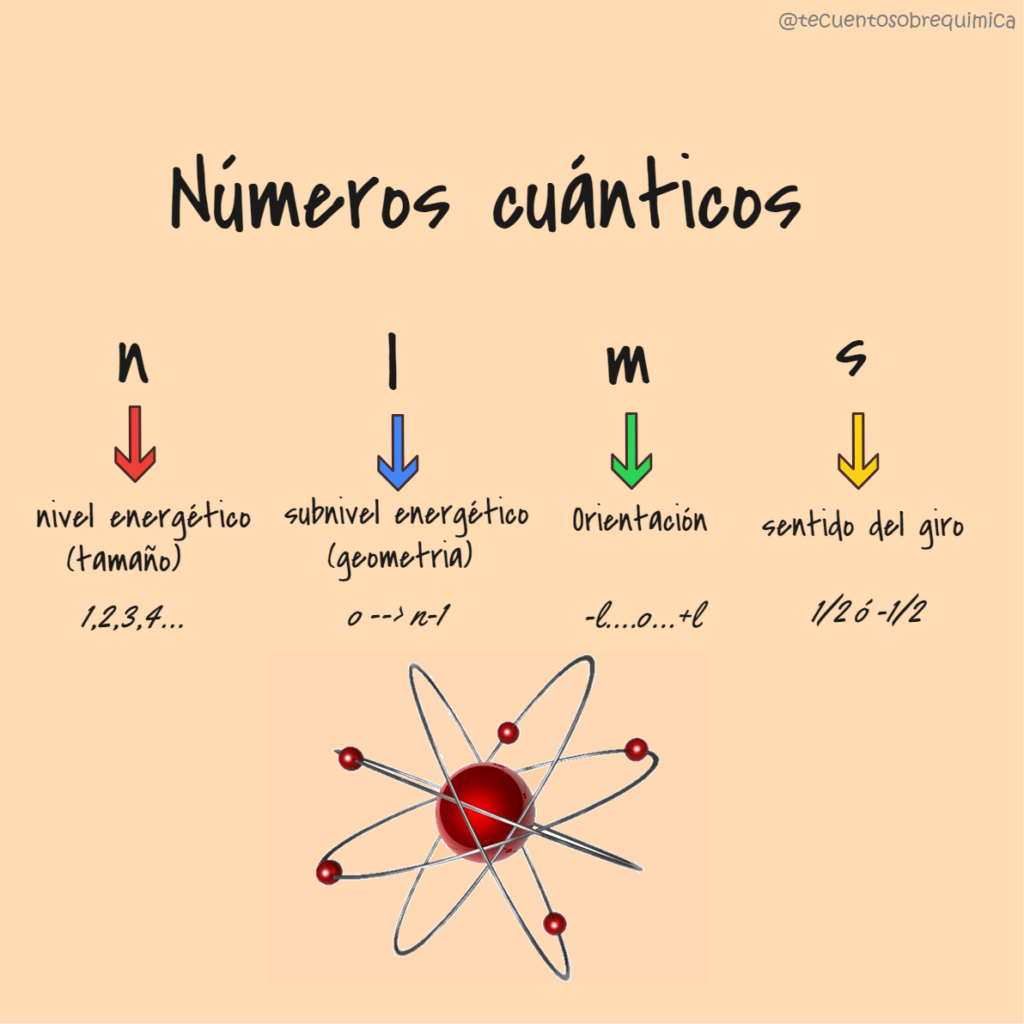
1. Número cuántico principal (n)
Indica el nivel principal de energía en el que se encuentra el electrón y su distancia aproximada al núcleo.
- Valores: 1, 2, 3, 4, 5, 6, 7…
- A mayor valor de n, mayor energía y mayor distancia del núcleo.
Ejemplo:
n = 1 → primer nivel
n = 3 → tercer nivel
2. Número cuántico secundario o azimutal (l)
Indica el subnivel de energía y la forma del orbital.
- Valores: desde 0 hasta n – 1
Relación con subniveles:
l = 0 → subnivel s
l = 1 → subnivel p
l = 2 → subnivel d
l = 3 → subnivel f
Ejemplo:
Si n = 3 → l puede ser 0, 1 o 2 → subniveles 3s, 3p y 3d
3. Número cuántico magnético (m o mₗ)
Indica la orientación del orbital en el espacio.
- Valores: desde -l hasta +l (incluyendo el 0)
Ejemplos:
Si l = 0 → m = 0
Si l = 1 → m = -1, 0, +1
Si l = 2 → m = -2, -1, 0, +1, +2
Esto permite conocer el número de orbitales:
Subnivel s → 1 orbital
Subnivel p → 3 orbitales
Subnivel d → 5 orbitales
Subnivel f → 7 orbitales
4. Número cuántico de espín (mₛ)
Indica el sentido de giro del electrón.
- Valores: +1/2 y -1/2
Esto explica que en un mismo orbital solo pueden existir dos electrones con espines opuestos.
RESUMEN: Veamos la información sintetizada en el siguiente recurso interactivo, volteando cada tarjeta:
Números Cuánticos
Haz clic en cada tarjeta para voltearla
EJEMPLO APLICADO
Electrón en el subnivel 2p:
n = 2 → segundo nivel
l = 1 → subnivel p
m = -1, 0 o +1 → tres orbitales posibles
mₛ = +1/2 o -1/2
Consolidación:
AIC: Trabajamos de forma individual en los siguientes EJERCICIOS
- ¿Qué número cuántico indica el nivel de energía?
- ¿Qué valores puede tomar l si n = 4?
- ¿Cuántos orbitales tiene el subnivel p?
- ¿Cuáles son los valores de m cuando l = 2?
- ¿Qué valores puede tomar el espín?
- Para un electrón en 3d, identifica los valores de n y l.
Sugerencia Rúbrica
RÚBRICA: RESUMEN
https://docs.google.com/spreadsheets/d/1AWYMzSl6BPYz6TqUBBPIPP3pYw_eSEPDg9uTExkgh7s/edit?gid=0#gid=0
NEE – Agregar el tipo de adaptaciones curriculares
Principio II: Pautas 6.1 – 6.3 – 6.4
Principio III: Pautas 7.1 – 8.1 – 9.1
ALUMNO 1: Constante monitoreo. Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 2: Constante monitoreo, Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 3: Constante monitoreo. Corroborar que el contenido entregado en clase haya sido comprendido por la estudiante mediante retroalimentación.
