La tabla periódica: Ubicación de los elementos químicos y sus propiedades

Destreza / Competencia:
CN.Q.5.1.6. Relacionar la estructura electrónica de los átomos con la posición en la tabla periódica, para deducir las propiedades químicas de los elementos.
CN.Q.5.1.12. Deducir y predecir la posibilidad de formación de compuestos químicos, con base en el estado natural de los elementos, su estructura electrónica y su ubicación en la tabla periódica.
¿En qué áreas de la vida se puede aplicar este contenido?
Los contenidos sobre la tabla periódica, la ubicación de los elementos y sus propiedades se aplican en la vida porque permiten entender, comparar y predecir el comportamiento de los elementos que forman los materiales y sustancias que usamos diariamente.
- Vida cotidiana: te ayudan a comprender por qué ciertos elementos se usan en cables, utensilios, medicamentos, fertilizantes, baterías, joyas y productos tecnológicos, según sus propiedades como conductividad, reactividad o dureza.
- Desarrollo personal: fortalecen tu capacidad de interpretar la organización de la materia, relacionando la posición de un elemento en la tabla con su comportamiento químico y sus posibles usos.
- Contexto social / académico: te permiten analizar temas como reacciones químicas, formación de compuestos, clasificación de materiales, propiedades periódicas y aplicaciones industriales, base importante para estudios posteriores en química, salud, ambiente, ingeniería y tecnología.
Actividades de aprendizaje:
Anticipación
“¿Qué tienen en común estos objetos?”
Muestra o menciona varios objetos cotidianos, por ejemplo: un cable de cobre, una lata de aluminio, una pila, una joya, un lápiz de grafito y una botella con cloro. Luego pregúntales:
- ¿De qué elementos creen que están hechos estos objetos?
- ¿Por qué unos materiales conducen electricidad, otros son frágiles y otros reaccionan con facilidad?
- ¿Creen que la posición de un elemento en la tabla periódica puede ayudar a explicar sus propiedades?
Después conecta sus respuestas explicando que la tabla periódica no solo organiza elementos, sino que también permite entender su ubicación, clasificación y propiedades, y predecir cómo se comportan en la vida real.
Construcción:
La tabla periódica de los elementos químicos:
La tabla periódica de los elementos es un registro de todos los elementos químicos conocidos por la humanidad. Los elementos están ordenados en forma de tabla según su número atómico (número de protones), su configuración electrónica y sus propiedades químicas.
En esta tabla los elementos están organizados en filas y columnas que muestran cierta periodicidad: los elementos que pertenecen a una misma columna tienen propiedades similares. En principio, toda la materia conocida del universo está compuesta por diversas combinaciones de los 118 elementos, registrados en la tabla periódica.
La tabla periódica es una herramienta fundamental para la química, la biología y otras ciencias naturales, que se actualiza con el pasar de los años, conforme aprendemos más sobre las propiedades de la materia y las relaciones entre los elementos.
¿Cómo está organizada la tabla periódica?
La tabla periódica actual está estructurada en siete filas (horizontales) denominadas períodos y en 18 columnas (verticales) llamadas grupos o familias. Los elementos químicos están ordenados en orden creciente de sus números atómicos, es decir, el número atómico aumenta de izquierda a derecha en el período y de arriba hacia abajo en el grupo.
Los dieciocho grupos conocidos son:
Grupo 1 (IA).
Los metales alcalinos: litio (Li), sodio (Na), potasio (K), rubidio (Rb), cesio (Cs), francio (Fr). Además en este grupo se encuentra el hidrógeno (H), que es un gas.
Grupo 2 (IIA)
Los metales alcalinotérreos: berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba), radio (Ra).
Grupo 3 (IIIB)
La familia del escandio (Sc), que incluye al Itrio (Y) y a las tierras raras: lantano (La), cerio (Ce), praseodimio (Pr), neodimio (Nd), prometio (Pm), samario (Sm), europio (Eu), gadolinio (Gd), terbio (Tb), disprosio (Dy), holmio (Ho), erbio (Er), tulio (Tm), iterbio (Yt), lutecio (Lu). También se incluyen a los actínidos: actinio (Ac), torio (Th), protactinio (Pa), uranio (U), neptunio (Np), plutonio (Pu), americio (Am), curio (Cm), berkelio (Bk), californio (Cf), einstenio (Es), fermio (Fm), mendelevio (Md), nobelio (No) y lawrencio (Lr).
Grupo 4 (IVB)
La familia del titanio (Ti), que incluye el circonio (Zr), el hafnio (Hf) y el rutherfordio (Rf), este último sintético y radiactivo.
Grupo 5 (VB)
La familia del vanadio (V): niobio (Nb), tántalo (Ta) y dubnio (Db), este último es sintético.
Grupo 6 (VIB)
La familia del cromo (Cr): molibdeno (Mb), wolframio (W) y seaborgio (Sg), este último es sintético.
Grupo 7 (VIIB)
La familia del manganeso (Mn): renio (Re), tecnecio (Tc) y bohrio (Bh), estos dos últimos son sintéticos.
Grupo 8 (VIIIB)
La familia del hierro (Fe): rutenio (Ru), osmio (Os) y hassio (Hs), este último sintético.
Grupo 9 (VIIIB)
La familia del cobalto (Co): rodio (Rh), iridio (Ir) y el sintético meitneiro (Mt).
Grupo 10 (VIIIB)
La familia del níquel (Ni): paladio (Pd), platino (Pt) y el sintético darmstadtio (Ds).
Grupo 11 (IB)
La familia del cobre (Cu): plata (Ag), oro (Au) y el sintético roentgenio (Rg).
Grupo 12 (IIB)
La familia del zinc (Zn): cadmio (Cd), mercurio (Hg) y el sintético copernicio (Cn).
Grupo 13 (IIIA).
Los térreos: boro (Br), aluminio (Al), galio (Ga), indio (In), talio (Tl) y el sintético nihonio (Nh).
Grupo 14 (IVA)
Los carbonoideos: carbono (C), silicio (Si), germanio (Ge), estaño (Sn), plomo (Pb) y el sintético flevorio (Fl).
Grupo 15 (VA)
Los nitrogenoideos: nitrógeno (N), fósforo (P), arsénico (As), antimonio (Sb), bismuto (Bi) y el sintético moscovio (Mc).
Grupo 16 (VIA)
Los calcógenos o anfígenos: oxígeno (O), azufre (S), selenio (Se), teluro (Te), polonio (Po) y el sintético livermorio (Lv).
Grupo 17 (VIIA)
Los halógenos: flúor (F), cloro (Cl), bromo (Br), yodo (I), astato (At) y el sintético teneso (Ts).
Grupo 18 (VIIIA)
Los gases nobles: helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe), radón (Rn) y el sintético oganesón (Og).
Todos estos grupos están contenidos en otros más grandes que tienen propiedades generales, descritos a continuación:
Metales
Son elementos que, en general, presentan brillo, buena conductividad térmica y eléctrica, y suelen ser maleables y dúctiles. En la tabla periódica incluyen los elementos de la izquierda y del centro: grupos 1 y 2 (excepto el hidrógeno), grupos 3 al 12 y parte de los grupos 13, 14, 15 y 16.
No metales
Son elementos que, en general, son malos conductores, no tienen brillo metálico y muchos se presentan como gases o sólidos frágiles. Se ubican principalmente en la parte superior derecha de la tabla e incluyen el hidrógeno, además de elementos de los grupos 14, 15, 16, 17 y 18.
Metaloides
Son elementos con propiedades intermedias entre metales y no metales; pueden comportarse como semiconductores. Se ubican en la “línea escalonada” que separa metales y no metales. Los más reconocidos son: boro (B), silicio (Si), germanio (Ge), arsénico (As), antimonio (Sb), telurio (Te) y, en algunas clasificaciones, polonio (Po) y astato (At).
HISTORIA DE LA TABLA PERIÓDICA:
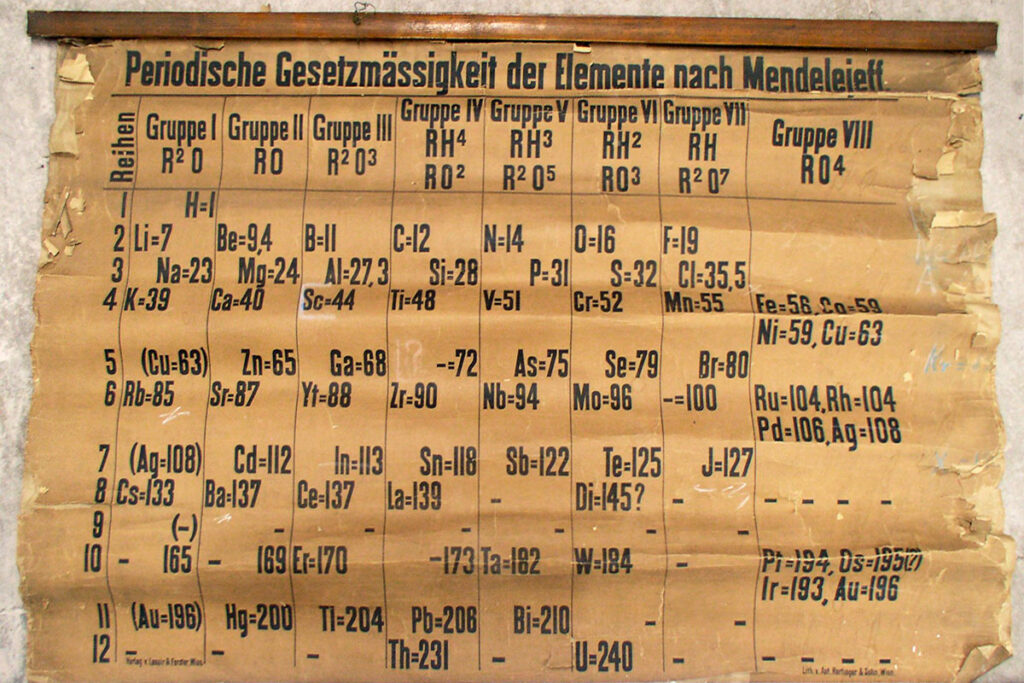
La primera versión de la tabla periódica fue publicada en 1869 por el profesor de química ruso Dmitri Mendeléyev, y contenía 63 de los 118 elementos hoy conocidos en la naturaleza y estaba organizada basándose en sus propiedades químicas. Por otra parte, el profesor de química alemán Julius Lothar Meyer publicó una versión ampliada, pero basándose en las propiedades físicas de los átomos. Ambos estudiosos organizaron los elementos en filas, teniendo la previsión de dejar espacios en blanco en donde intuían que habría elementos aún por descubrir.
En 1871 Mendeléyev publicó otra versión de la tabla periódica que agrupaba los elementos según sus propiedades comunes en columnas enumeradas desde la I hasta la VIII conforme al estado de oxidación del elemento.
Finalmente, en 1923 el químico americano Horace Groves Deming publicó una tabla periódica con 18 columnas identificadas que constituye la versión utilizada actualmente.
Consolidación:
Práctica de laboratorio sugerida.
Sugerencia Rúbrica
RÚBRICA: Enlace de la rúbrica donde deben estar todos los criterios detallados y deben ser calificados sobre 10 o cuales son los indicadores a evaluar en el caso de no tener calificación.
https://docs.google.com/spreadsheets/d/1AWYMzSl6BPYz6TqUBBPIPP3pYw_eSEPDg9uTExkgh7s/edit?gid=0#gid=0
PRÁCTICA DE LABORATORIO SUGERIDA:
Llevamos a cabo el desarrollo de la determinación de algunas propiedades físicas de elementos químicos.
Nos basamos en las instrucciones dadas en la GUÍA DE PRACTICAS DE LABORATORIO que está adjunta al QUIMIOKIT, y observamos el siguiente material audiovisual para seguir sus instrucciones:
Después de haber desarrollado los experimentos, elaboramos el informe correspondiente (en la guía de prácticas de laboratorio), lo revisamos y calificamos con la RÚBRICA DE INFORMES DE PRÁCTICAS DE LABORATORIO, la misma que fue socializada anteriormente y facilitada a los alumnos en Classroom.
NEE – Agregar el tipo de adaptaciones curriculares
Principio II: Pautas 6.1 – 6.3 – 6.4
Principio III: Pautas 7.1 – 8.1 – 9.1
ALUMNO 1: Constante monitoreo. Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 2: Constante monitoreo, Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 3: Constante monitoreo. Corroborar que el contenido entregado en clase haya sido comprendido por la estudiante mediante retroalimentación.
