
Destreza / Competencia:
CN.Q.5.1.6. Relacionar la estructura electrónica de los átomos con la posición en la tabla periódica, para deducir las propiedades químicas de los elementos.
¿En qué áreas de la vida se puede aplicar este contenido?
Los contenidos sobre tendencias periódicas se aplican en la vida porque permiten predecir cómo se comportan los elementos según su posición en la tabla periódica.
- Vida cotidiana: te ayudan a entender por qué algunos elementos reaccionan más fácilmente, otros forman iones con mayor facilidad y otros se usan en materiales conductores, baterías, medicamentos o productos de limpieza.
- Desarrollo personal: fortalecen tu capacidad de relacionar la posición de un elemento con sus propiedades, comprendiendo por qué cambian el tamaño atómico, la electronegatividad o la energía de ionización.
- Contexto social / académico: te permiten interpretar mejor la formación de enlaces, la reactividad química, la clasificación de elementos y el comportamiento de compuestos, base para estudios posteriores en química, biología, medicina, ambiente e ingeniería.
Actividades de aprendizaje
Anticipación
Construcción: tiempo
PROPIEDADES PERIÓDICAS
Las propiedades periódicas son características de los elementos que varían de manera regular a medida que avanzamos en la tabla periódica. Estas variaciones dependen principalmente del número atómico y de la distribución de los electrones en los niveles de energía.
Estudiarlas permite predecir cómo se comporta un elemento, qué tan reactivo puede ser y cómo se relaciona con otros.
La tabla periódica no solo organiza elementos: también permite predecir sus propiedades.
Por eso se dice que las propiedades son periódicas, porque se repiten o cambian siguiendo un patrón regular.
Vamos a prender cuáles son estas propiedades y cómo varían dentro de la tabla periódica:
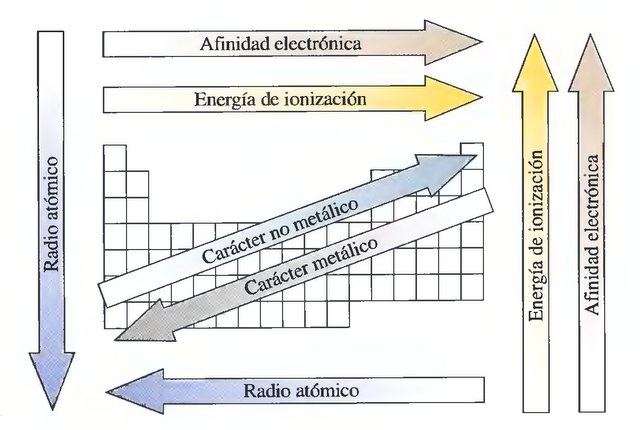
1. Radio atómico
Es el tamaño aproximado de un átomo, es decir, la distancia desde el núcleo hasta la región más externa donde se encuentran los electrones.
Tendencia en la tabla periódica:
- Aumenta de arriba hacia abajo en un grupo, porque hay más niveles de energía.
- Disminuye de izquierda a derecha en un período, porque aumenta la carga nuclear y los electrones son atraídos con más fuerza hacia el núcleo.
Ejemplo:
El potasio (K) tiene mayor radio atómico que el sodio (Na).
2. Radio iónico
Es el tamaño que tiene un átomo cuando gana o pierde electrones y se convierte en ion.
- Si un átomo pierde electrones, forma un catión y su radio disminuye.
- Si un átomo gana electrones, forma un anión y su radio aumenta.
Ejemplo:
- Na → Na⁺: el ion sodio es más pequeño que el átomo neutro.
- Cl → Cl⁻: el ion cloruro es más grande que el átomo neutro.
3. Energía de ionización
Es la cantidad de energía necesaria para arrancar un electrón de un átomo en estado gaseoso.
Tendencia:
- Aumenta de izquierda a derecha en un período.
- Disminuye de arriba hacia abajo en un grupo.
Esto ocurre porque los electrones más cercanos al núcleo están más fuertemente atraídos.
Ejemplo:
El helio y el neón tienen energías de ionización muy altas.
4. Afinidad electrónica
Es la energía liberada o absorbida cuando un átomo gaseoso gana un electrón.
En términos escolares, se interpreta como la tendencia de un átomo a aceptar electrones.
Tendencia general:
- Aumenta de izquierda a derecha.
- Disminuye de arriba hacia abajo.
Los no metales, especialmente los halógenos, tienen alta afinidad electrónica.
Ejemplo:
El cloro tiene gran tendencia a ganar un electrón.
5. Electronegatividad
Es la capacidad que tiene un átomo para atraer hacia sí los electrones de un enlace químico.
Tendencia:
- Aumenta de izquierda a derecha.
- Disminuye de arriba hacia abajo.
El elemento más electronegativo es el flúor (F).
Importancia:
Sirve para predecir el tipo de enlace químico y la polaridad de las moléculas.
6. Carácter metálico
El carácter metálico es la tendencia de un elemento a perder electrones y comportarse como metal.
Tendencia:
- Aumenta de arriba hacia abajo.
- Aumenta de derecha a izquierda.
Por eso, los elementos más metálicos están en la parte inferior izquierda de la tabla.
Ejemplo:
El cesio (Cs) y el francio (Fr) presentan alto carácter metálico.
7. Carácter no metálico
Es la tendencia de un elemento a ganar electrones y comportarse como no metal.
Tendencia:
- Aumenta de izquierda a derecha.
- Aumenta de abajo hacia arriba.
Los no metales más marcados están en la parte superior derecha de la tabla, excepto los gases nobles.
TODAS ESTAS TENDENCIAS ESTÁN RESUMIDAS EN EL SIGUIENTE RECURSO INTERACTIVO:
Tendencias periódicas
Selecciona una dirección para explorar cómo cambian las propiedades.
Selecciona una dirección para ver cómo cambian las propiedades.
Importancia de las propiedades periódicas
Estas propiedades permiten:
- comparar elementos químicos,
- predecir su comportamiento,
- entender por qué reaccionan de manera distinta,
- explicar la formación de iones y enlaces químicos.
Consolidación:
“Carrera de tendencias periódicas”
Objetivo: consolidar la comprensión de las propiedades periódicas y sus tendencias en la tabla periódica.
Cómo aplicarla:
- Forma equipos de 3 o 4 estudiantes.
- Entrega a cada equipo una tabla periódica muda y una lista de propiedades:
- radio atómico
- energía de ionización
- afinidad electrónica
- electronegatividad
- carácter metálico
- Cada equipo debe:
- escribir con flechas hacia dónde aumenta cada propiedad en la tabla,
- escoger 2 elementos y compararlos usando una propiedad,
- justificar oralmente cuál tiene mayor o menor valor.
Ejemplos de comparación:
- Na vs Cl → electronegatividad
- K vs Li → radio atómico
- Mg vs Al → energía de ionización
- F vs Cs → carácter no metálico / metálico
Cierre:
Tú dices una propiedad y los grupos levantan rápidamente su tabla señalando la dirección correcta. Luego preguntas:
“¿Qué elemento tendría mayor valor y por qué?”
Por qué funciona:
Es sencilla, rápida y les obliga a visualizar, comparar y justificar las tendencias, no solo memorizarlas.
Sugerencia Rúbrica
RÚBRICA: Resúmenes
https://docs.google.com/spreadsheets/d/1AWYMzSl6BPYz6TqUBBPIPP3pYw_eSEPDg9uTExkgh7s/edit?gid=0#gid=0
NEE – Agregar el tipo de adaptaciones curriculares
Principio II: Pautas 6.1 – 6.3 – 6.4
Principio III: Pautas 7.1 – 8.1 – 9.1
ALUMNO 1: Constante monitoreo. Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 2: Constante monitoreo, Dar tiempo adicional para el desarrollo de la actividad y se reduce el número de ejercicios o se modifican los ejercicios con un nivel de dificultad reducido, de acuerdo con sus necesidades académicas.
ALUMNO 3: Constante monitoreo. Corroborar que el contenido entregado en clase haya sido comprendido por la estudiante mediante retroalimentación.
